1. Общие рекомендации. Назначают токолитическую терапию. Кроме того, если вероятность сохранения беременности невелика и высок риск рождения глубоко недоношенного ребенка, назначают препараты, ускоряющие созревание легких плода. Есть сообщения о том, что эффективность токолитической терапии повышается при проведении эмпирической антимикробной терапии. После 34 нед беременности токолитические средства не назначают, поскольку дети рождаются жизнеспособными, а риск осложнений токолитической терапии значительно превосходит пользу от ее применения.
2. Токолитические средства — группа препаратов с разным механизмом действия, подавляющих сократительную активность матки. К ним относятся бета-адреностимуляторы, сульфат магния, НПВС (угнетают синтез простагландинов) и антагонисты кальция. Из всех препаратов только бета-адреностимулятор ритодрин одобрен FDA в качестве токолитического средства. Тем не менее в США помимо ритодрина широко применяют сульфат магния и тербуталин. Также имеются сообщения об использовании в качестве токолитических средств индометацина и нифедипина, однако опыт их применения в акушерстве невелик.
Токолитические средства в большинстве случаев назначают в режиме монотерапии. Необходимо остановить или значительно снизить сократительную активность матки. Лечение обычно начинают с бета-адреностимуляторов (ритодрина или тербуталина) либо с сульфата магния. Если препарат неэффективен в максимальной дозе, его заменяют другим с иным механизмом действия. Эффективность второго препарата наблюдается в 10—20% случаев.
а. Бета-адреностимуляторы. Для токолитической терапии используют ритодрин, тербуталин, гексопреналин, изоксуприн и сальбутамол. Хотя только ритодрин одобрен FDA для токолитической терапии, в США широко применяют тербуталин. Бета-адреностимуляторы вызывают повышение концентрации цАМФ с последующим снижением концентрации ионов кальция в цитоплазме. В результате снижается активность киназы легких цепей миозина и снижается сократимость миометрия.
1) Побочное действие бета-адреностимуляторов включает тахикардию, одышку, боль в груди, а также гипергликемию и гипокалиемию.
2) Противопоказания — ИБС и другие болезни сердца, которые могут обостриться на фоне тахикардии, тиреотоксикоз, артериальная гипертония. Относительное противопоказание — сахарный диабет. Применение бета-адреностимуляторов при этом заболевании допускается только при тщательном контроле уровня глюкозы плазмы. При гипергликемии повышают дозу инсулина.
3) Дозы и применение. При лечении бета-адреностимуляторами может развиться РДСВ. Причины, вероятнее всего, связаны с инфекцией, а не с самими токолитическими средствами. Тем не менее на время токолитической терапии потребление жидкости ограничивают до 100 мл/ч. Есть сообщения о том, что для профилактики РДСВ следует использовать гипотонические растворы.
а) Ритодрин вводят внутрь или в/в. Для быстрого прекращения схваток рекомендуется в/в введение. В/в ритодрин вводят в 5% глюкозе со скоростью 0,05—0,1 мг/мин. Скорость введения увеличивают каждые 15—30 мин на 0,05 мг/мин до прекращения схваток. После прекращения схваток лечение продолжают еще в течение 12—24 ч. Скорость введения не должна превышать 0,35 мг/мин. При проявлении побочного действия препарата ее снижают. При возникновении боли в груди введение препарата приостанавливают и проводят ЭКГ. Если ЧСС превышает 130 мин-1, дозу ритодрина снижают. Внутрь ритодрин вначале назначают в дозе 10 мг каждые 2 ч, а затем — по 10—20 мг каждые 4—6 ч.
б) Тербуталин применяют как для лечения, так и для профилактики преждевременного начала родовой деятельности. С профилактической целью тербуталин обычно назначают внутрь, а для остановки родовой деятельности — в/в. Следует подчеркнуть, что для остановки родовой деятельности тербуталин менее эффективен, чем ритодрин. Некоторые авторы рекомендуют п/к введение тербуталина с помощью инфузионного насоса по 0,25 мг каждый час до прекращения схваток. Затем препарат назначают внутрь в дозе 2,5—5,0 мг каждые 4—6 ч. Во время лечения следят, чтобы ЧСС у беременной не превышала 130 мин-1. Некоторые авторы рекомендуют подбирать дозу тербуталина так, чтобы ЧСС превышала исходную не более чем на 20—25%.
б. Сульфат магния
1) Механизм токолитического действия точно не установлен. Известно, что сульфат магния снижает возбудимость и сократимость миометрия за счет уменьшения концентрации ионов кальция в цитоплазме мышечных клеток.
2) Дозы и применение
а) Противопоказания включают нарушения внутрисердечной проводимости, миастению и тяжелую сердечную недостаточность. Относительное противопоказание — ХПН, поскольку препарат выводится преимущественно почками. При лечении сульфатом магния возможно угнетение дыхания — во время лечения тщательно следят за дыханием беременной. Это особенно важно при одновременном назначении наркотических анальгетиков, седативных и других лекарственных средств, угнетающих дыхание.
б) Введение препарата. 4—6 г сульфата магния растворяют в 100 мл физиологического раствора и вводят в/в в течение 30—45 мин, после чего переходят на непрерывное в/в введение со скоростью 2—4 г/ч до прекращения или значительного урежения схваток. Иногда после прекращения родовой деятельности незначительные сокращения матки продолжаются. В этом случае регулярно проводят влагалищное исследование. Если раскрытие шейки матки продолжается, дозу увеличивают или назначают другое токолитическое средство.
в) Терапевтическая концентрация препарата в сыворотке составляет 5,5—7,5 мг%. Для ее достижения в большинстве случаев достаточно вводить сульфат магния со скоростью 3—4 г/ч. Признаки передозировки — угнетение сухожильных рефлексов и дыхания. Угнетение сухожильных рефлексов возникает при концентрации магния в сыворотке 7—10 мг%, угнетение дыхания — при концентрации выше 12 мг%.
г) Если лечение неэффективно или требуются высокие дозы сульфата магния, определяют концентрацию магния в сыворотке. Если она ниже терапевтической (вследствие быстрого выведения магния почками), допустимо повышение дозы. Если при терапевтической концентрации магния в сыворотке эффекта не наблюдается, назначают другой препарат (одновременно с сульфатом магния или вместо него).
д) При наличии у беременной ХПН дозу сульфата магния снижают. Во время лечения тщательно следят за уровнем магния сыворотки.
3) Побочное действие наблюдается реже, чем при лечении другими токолитическими средствами. Возможны приливы (обычно в начале лечения), сердцебиение, головная боль и сухость во рту. Иногда наблюдаются диплопия и нарушение аккомодации. При назначении сульфата магния после массивной инфузионной терапии или бета-адреностимуляторов возможен отек легких.
а) Передозировка сульфата магния встречается довольно часто. Она проявляется угнетением дыхания и падением мышечного тонуса. Для устранения симптомов вводят глюконат кальция в/в медленно. При значительном угнетении дыхания может потребоваться ИВЛ.
в. НПВС считаются эффективными токолитическими средствами. Они могут вызвать преходящее маловодие, но в течение 1—2 сут после отмены препарата объем околоплодных вод нормализуется. Также сообщалось, что НПВС вызывают сужение артериального протока у плода. Риск этого осложнения наиболее высок при приеме препаратов до 32-й недели беременности. Через 24 ч после отмены препарата проходимость артериального протока полностью восстанавливается.
1) Выбор препарата. НПВС применяют при неэффективности или противопоказаниях к использованию других токолитических средств. Перед началом лечения беременную предупреждают о риске сужения артериального протока у плода и обсуждают возможность других методов лечения.
2) Противопоказания включают аллергию к салицилатам, аспириновую бронхиальную астму, нарушения гемостаза, а также тяжелую ХПН и печеночную недостаточность. Относительное противопоказание — язвенная болезнь.
3) Индометацин хорошо всасывается при приеме внутрь и ректальном введении. В связи с тем что при регулярной родовой деятельности эвакуация содержимого желудка замедлена, индометацин лучше вводить ректально. Вначале вводят 100 мг, а затем по 50 мг каждые 8 ч в течение 48 ч. Поскольку визуализация артериального протока с помощью УЗИ затруднена, для ранней диагностики его сужения у плода проводят непрерывную КТГ. Ежедневно определяют объем околоплодных вод. При подозрении на маловодие индометацин отменяют.
4) Побочное действие наблюдается редко. Есть сообщения о том, что НПВС повышают риск послеродового кровотечения. В связи с этим на сроке беременности более 32 нед НПВС противопоказаны.
г. Антагонисты кальция нарушают проникновение ионов кальция в клетку, снижая таким образом сократимость клеток миометрия. Проспективные исследования антагониста кальция нифедипина показали, что он не оказывает неблагоприятного влияния на плод и по эффективности приближается к ритодрину. Препарат назначают в дозе 10 мг, обычно под язык. Нифедипин принимают повторно в той же дозе каждые 15—20 мин до прекращения схваток (не более 3 доз). После прекращения схваток нифедипин назначают по 10 мг каждые 6 ч в течение нескольких суток.
Дополнительные рекомендации. Несмотря на широкое применение разных токолитических средств, распространенность преждевременных родов в западных странах не изменилась. Причина этого, вероятно, заключается в поздней диагностике преждевременных родов.
1. Монотерапия. Рекомендуется следующий порядок назначения препаратов. Лечение начинают с бета-адреностимуляторов или сульфата магния. Если ни то, ни другое неэффективно, назначают НПВС или антагонисты кальция. Несмотря на сообщения об эффективности токолитических средств перечисленных групп, ни одно из них не изучено настолько, чтобы стать препаратом выбора.
2. Комбинированная терапия токолитическими средствами показана только в самых крайних случаях, например на сроке беременности до 28—30 нед при неэффективности монотерапии и раскрытии шейки матки более чем на 2—3 см. Продление беременности хотя бы на 2 сут в этом случае позволяет ускорить созревание легких плода и значительно снизить риск гибели новорожденного. Показано, что каждый дополнительный день внутриутробного пребывания на сроке беременности 25—28 нед значительно повышает жизнеспособность новорожденного. При одновременном назначении нескольких токолитических средств женщине подробно разъясняют вероятные последствия, а также возможность других методов лечения.
Неэффективность токолитических средств часто обусловлена инфекцией. При хориоамнионите токолитическая терапия противопоказана. При других инфекциях, например пиелонефрите, токолитическая терапия допустима, однако при этом повышается риск РДСВ. Для профилактики РДСВ ограничивают прием и введение жидкостей (до 100 мл/ч). При лечении кортикостероидами в течение 24—36 ч может наблюдаться лейкоцитоз до 30 000 мкл-1 со сдвигом лейкоцитарной формулы влево. При уровне лейкоцитов более 30 000 мкл-1 исключают инфекцию.
а. Идеальной комбинации токолитических средств не существует. Наиболее эффективно сочетание индометацина с сульфатом магния или ритодрином. Также сообщалось о применении ритодрина в сочетании с сульфатом магния, однако эффективность этой схемы практически не отличалась от таковой при использовании каждого препарата в отдельности. Антагонисты кальция не рекомендуется сочетать с другими препаратами.
б. Одновременное назначение трех токолитических средств не рекомендуется, поскольку это значительно увеличивает риск осложнений, не повышая эффективность лечения.
3. РДСВ — частое осложнение токолитической терапии. Ранее считалось, что он обусловлен применением кортикостероидов для ускорения созревания легких плода, но исследования показали, что основная причина РДСВ при преждевременных родах — инфекция. Профилактика включает ограничение жидкости. Общее потребление жидкости (внутрь и в/в) не должно превышать 100—125 мл/ч или примерно 2,0—2,5 л/сут. При лечении токолитическими средствами для инфузионной терапии используют 5% глюкозу или 0,25% NaCl.
4. Ускорение созревания легких плода
а. Кортикостероиды. В 1994 г. Национальный институт здоровья США рекомендовал кортикостероиды для ускорения созревания легких плода при угрозе преждевременных родов до 34-й недели беременности. Механизм действия кортикостероидов в этом случае точно не установлен. Возможно, они активируют ферменты, участвующие в синтезе сурфактанта, либо стимулируют высвобождение сурфактанта из альвеолоцитов II типа. Было установлено, что кортикостероиды наиболее эффективны на 30—34-й неделе беременности. Среди новорожденных наибольший эффект лечения был отмечен у негритянских девочек, а наименьший — у белых мальчиков. После 34 нед беременности кортикостероиды неэффективны. Обычно назначают бетаметазон, 12 мг внутрь с интервалом 12—24 ч (общая доза 24 мг), или дексаметазон, 5 мг внутрь каждые 6 ч (общая доза 20 мг). Лечение начинают за 24—48 ч до родоразрешения.
б. Другие методы. Развитие и созревание легких плода достаточно сложны. Как показали исследования, важную роль в этом процессе играют T4 и пролактин. Было обнаружено, что назначение бетаметазона в сочетании с протирелином более эффективно для профилактики болезни гиалиновых мембран, чем монотерапия бетаметазоном. Хотя такая схема лечения еще широко не применяется, если высок риск рождения глубоко недоношенного ребенка, ее назначение допустимо.
5. Антимикробная терапия. Одной из главных причин преждевременных родов считают инфекцию. Согласно исследованиям, антимикробная терапия значительно повышает эффективность профилактики преждевременных родов. Однако из-за дороговизны и сложности массового обследования беременных этот метод не нашел широкого применения. Кроме того, есть сведения о неэффективности ампициллина в сочетании с эритромицином при преждевременном начале родовой деятельности. Некоторые авторы сообщали об эффективном применении профилактической антимикробной терапии у беременных с невыясненными причинами преждевременного начала родовой деятельности. После взятия материала из канала шейки матки на посев в этом случае назначают ампициллин, 2 г в/в 4 раза в сутки. Лечение продолжают в течение 48 ч и, если результат посева отрицательный, антибиотик отменяют. При аллергии к пенициллинам, назначают цефалоспорины, действующие на Streptococcus agalactiae. По данным других авторов, ампициллин при преждевременном начале родовой деятельности неэффективен.
6. Кровоизлияние в желудочки мозга чаще возникает у детей, рожденных до 32—34-й недели беременности. Профилактика включает введение роженице фитоменадиона, 10 мг в/м.
Поддерживающая токолитическая терапия. После прекращения регулярных схваток токолитическую терапию продолжают в течение 12—24 ч в минимальной дозе, достаточной для сохранения нормального тонуса матки. После этого переходят на поддерживающее лечение. Было отмечено, что поддерживающая токолитическая терапия не продляет беременность (на фоне плацебо беременность удалось продлить на 36 сут, а при приеме ритодрина внутрь — на 34 сут), однако предупреждает повторное возникновение преждевременной родовой деятельности. В настоящее время используют разные схемы поддерживающей токолитической терапии. Однако проспективных исследований эффективности этого метода лечения не проводилось.
1. Бета-адреностимуляторы. Применяют ритодрин, 10—20 мг внутрь каждые 4—6 ч, или тербуталин, 2,5—5,0 мг внутрь каждые 4—6 ч. Бета-адреностимуляторы вызывают тахикардию, поэтому перед каждым приемом беременная должна определять ЧСС. Если ЧСС больше 115 мин-1, прием препарата следует отложить. Тербуталин может нарушать толерантность к глюкозе. Беременным, принимающим бета-адреностимуляторы в течение длительного времени, обязательно проводят одночасовой пероральный тест на толерантность к глюкозе с 50 г глюкозы. Для поддерживающей токолитической терапии применяют также глюконат магния внутрь и п/к введение тербуталина с помощью инфузионного насоса.
2. Глюконат магния, согласно исследованиям Martin с соавт., при назначении в дозе 1 г внутрь каждые 2—4 ч по эффективности не уступает ритодрину и несколько реже вызывает побочные эффекты. При длительном применении возможно угнетение секреции ПТГ и снижение уровня кальция в сыворотке. Насколько влияет последнее на сократительную активность матки, остается неясным.
И провести необходимое лечение.
Профилактика сводится к наблюдению за беременной, своевременному выделению групп риска по преждевременным родам, диагностированию и лечению возникающих нарушений (инфекции, истмико-цервикальной недостаточности (ИЦН), сопутствующей экстрагенитальной патологии, рофилактику плацентарной недостаточности с ранних сроков беременности).
На основании письма Минздравсоцразвития РФ от 16.12.2011 №15-4/10/2-12700 «О направлении методического письма «Преждевременные роды»» профилактика преждевременных родов заключается в следующем:
Первичная профилактика
Эффективно :
- ограничение повторных внутриматочных манипуляций (диагностическое выскабливание матки во время медицинского аборта);
- информирование общественности о повышенном риске преждевременного рождения детей, зачатых с помощью вспомогательных репродуктивных технологий (ЭКО). Ограничение количества переносимых эмбрионов в зависимости от возраста пациентки и прогноза.
Неэффективно :
- прием поливитаминов до зачатия и на протяжении первых двух месяцев беременности.
Вторичная профилактика
Эффективно :
- внедрение антиникотиновых программ среди беременных.
Неэффективно :
- назначение белково-энергетических пищевых добавок в период беременности;
- дополнительный прием кальция во время беременности;
- дополнительный прием антиоксидантов - витаминов C и E;
- постельный режим;
- гидратация (усиленный питьевой режим, инфузионная терапия), используемая в целях нормализации фетоплацентарного кровотока для предотвращения преждевременных родов.
На сегодняшний день спорно в качестве профилактики:
- использование цервикального пессария;
- лечение заболеваний пародонта во время беременности.
Отдельные методы профилактики в группе беременных высокого риска преждевременных родов
Швы на шейку матки . Считается неэффективным наложение швов при короткой шейке матки всем беременным, кроме женщин из группы высокого риска преждевременных родов. Однако при длине шейки матки 15 мм и менее при дополнительном интравагинальном введении прогестерона частота преждевременных родов уменьшается.
При беременности двойней наложение швов на укороченную шейку матки, наоборот, повышает риск преждевременных родов.
Назначение прогестерона . Эффективно назначение прогестерона в группе высокого риска (прежде всего среди женщин, в анамнезе которых имеются преждевременные роды) снижает риск повторных преждевременных родов на 35%. Исследования показали, что еженедельные инъекции этого гормона, начиная с 16-ой – 20-ой недели и продолжая до 36-ой недели, значительно снижают риск повторных преждевременных родов для женщин в такой ситуации. Следует отметить, что прогестерон и его производные неэффективны при многоплодной беременности.
При назначении препаратов прогестерона необходимо информированное согласие женщины, поскольку компаниями-производителями при регистрации указанных лекарственных средств на территории Российской Федерации в показаниях к применению не указаны угрожающие преждевременные роды и возможность использования препаратов во втором и третьем триместрах беременности.
Антибактериальная профилактика . Выявление и лечение бессимптомной бактериурии (присутствие бактерий в моче более 10 КОЕ/мл). Лечение бактериального вагиноза у беременных с преждевременными родами в прошлом. Лечение бактериального вагиноза и хламидийной инфекции, проведенное на сроке беременности менее 20 недель, может снизить риск преждевременных родов.
Преждевременные роды неблагоприятны для ребёнка. При появлении болей внизу живота, напряжении матки, подозрении на излитие вод следует немедленно обратиться к врачу. Рекомендации к госпитализации следует выполнять неукоснительно.
Чем раньше беременная женщина обратилась к врачу, чем раньше было начато комплексное лечение, тем больше шансов, что удастся предотвратить роды раньше срока и родить здорового малыша.
Преждевременные роды пугают многих будущих мам. Многие авторы имеют различные мнения относительно определения данного понятия. Если брать в среднем зарубежный и российский опыт, то преждевременными считаются роды, срок которых наступил после 20 недели беременности, но до 37. Известно, что некоторые женщины имеют повышенный риск возникновения данной ситуации. Давайте рассмотрим в подробностях, какие факторы могут ее спровоцировать.
Риск преждевременных родов
Риск повышается у женщин:

Причины со стороны плода:
- внутриутробная гибель;
- задержка внутриутробного развития;
- врожденные аномалии.
Симптомы и признаки преждевременных родов
- диарея, которая имеет постоянный или периодический характер (ее может и не быть);
- тупая боль в пояснице - может быть постоянной или прерывистой;
- или их излитие;
- ощущение давления в тазовой области - живот опустился и ребенок давит предлежащим местом в область таза;
- схваткообразные боли внизу живота или по всему его периметру;
- изменение влагалищных выделений (на розовые или коричневые);
- схватки каждые 10 минут или меньше, которые могут сопровождаться болью.
Если ваш гинеколог считает, что у вас повышенный риск возникновения преждевременных родов, вы должны обязательно подготовиться и знать, как считать схватки. Схватки не всегда имеют болезненный характер. Иногда они проявляются, как окаменение живота на некоторое время. Вы можете потрогать живот и он будет в этот момент достаточно твердый и находиться в тонусе. Если вы узнали свои ощущения и они появляются каждые 10 минут или даже чаще, нужно как можно быстрее обратиться к гинекологу или в роддом для получения дальнейших инструкций.
Преждевременные роды - профилактика и лечение
 Хотя не все преждевременные роды можно предотвратить, существует ряд действий, которые способны уменьшить риск их наступления.
Хотя не все преждевременные роды можно предотвратить, существует ряд действий, которые способны уменьшить риск их наступления.
- Пейте много воды - от 8 до 10 стаканов в день. Обезвоживание может вызвать сокращения матки, что может привести к началу родовой деятельности.
- Опорожняйте мочевой пузырь каждые 2-3 часа, не реже. Полный мочевой может раздражать матку и вызывать ее сокращения.
- Избегайте подъема тяжестей и перенапряжения. Если у вас есть старшие дети, позволяйте сидеть у вас на коленях и выражайте любовь любыми другими способами, кроме ношения их на руках.
- В течение дня делайте частые перерывы и отдыхайте, желательно на левом боку. Данная поза способствует хорошему притоку крови к ребенку.
- Избегайте стимуляции груди и сексуальной активности.
При угрозе преждевременных родов обязательно возьмут мазок для определения возможной инфекции. В большинстве случаев определяются стрептококки группы B (Б). Беременной, у которой нет аллергии на пенициллин, будут назначены Пенициллин G или Ампициллин. Если у женщины аллергия на данные препараты и
- низкий риск анафилаксии, выбор упадет на Цефазолин;
- высокий риск анафилаксии, то Клиндамицин или Эритромицин, если бактерии показывают восприимчивость к данным препаратам, а если проверить это невозможно на данный момент, то выбирают Ванкомицин.
Женщинам, у которых риск рождения ребенка раньше времени очень высок, начиная со 2 триместра и до самых родов может быть рекомендовано принимать Прогестин.
Многие роды, которые начинаются раньше времени, у врачей получается остановить. Если родовая деятельность только начинается, то существуют лекарства (токолитики), которые способны остановить сокращение матки, хотя их применение и является рискованным делом. Токолитики включают сульфат магния, блокатор кальциевых каналов или, если роды начались раньше 32 недели, ингибиторы простагландинов. Последние противопоказаны позже 32 недели беременности, потому что могут вызвать кратковременное маловодие, преждевременное сужение или закрытие артериального протока.
Далее женщине введут внутримышечно кортикостероиды (бетаметазон или дексаметазон). Они нужны, чтобы ускорить созревание легких плода, снижения риска внутричерепного кровотечения и смертности. Данное лечение применяют до 34 недели беременности.
Получается следующая схема: для начала специалисты задерживают роды токолитиками, чтобы успели подействовать кортикостероиды.
Прогнозы для ребенка
Если преждевременные роды не остановить с помощью медицинского вмешательства, то ребенок родится недоношенный. Чем раньше это случится, тем больший риск для здоровья малыша. Большинство недоношенных детей нуждаются в особом уходе в отделении интенсивной терапии новорожденных.
У детей, рожденных раньше срока, имеются следующие признаки:

Для цитирования:
Серов В.Н., Сухорукова О.И. Профилактика преждевременных родов // РМЖ. Мать и дитя. 2014. №1. С. 3
До 2012 г. в России под понятием «рождение живого ребенка (новорожденного)» понималось «полное выделение или извлечение из организма матери плода при сроке беременности 28 недель и больше» (приказ МЗ СССР 12.06.86 г. № 848, приложение 1, п. 3).
В 2012 г. Минздрав России, «согласно Международной конвенции о правах ребенка, Декларации об обеспечении выживания, защиты и развития детей», отменил действие этой инструкции на территории Российской Федерации. С января 2012 г. в Российской Федерации введены критерии, рекомендованные Всемирной организацией здравоохранения (приказ МЗ РФ № 318 от 04.12.2011 г.). Критерии жизнеспособности плода: срок - 22 нед. и более, масса тела - 500 г и более. Среди рожденных в 22-23 нед. выживают 20% (каждый 5-й новорожденный), в 26 нед. - 60%, в 27-28 нед. - около 80% недоношенных новорожденных . Почти 100% выживаемость отмечена среди новорожденных в 32 нед. беременности и более. На долю недоношенных детей приходится 60-70% ранней неонатальной смертности и 65-75% детской смертности . Мертворождаемость при преждевременных родах в 8-13 раз выше, чем при своевременных . Дети, рожденные с массой менее 1500 г, в 200 раз чаще умирают новорожденными и, если выживают, в 10 раз чаще имеют неврологические и соматические осложнения, чем дети, рожденные с массой более 2500 г .
Ведущими причинами преждевременных родов до 28-недельного срока являются: инфекция, преждевременное излитие околоплодных вод и истмико-цервикальная недостаточность с последующим пролабированием и инфицированием оболочек плодного пузыря . По данным литературы, от 30 до 40% преждевременных родов обусловлены наличием инфекционного процесса [Власова Т.А., Вальдман С.Ф., Иванова Н.В., 2008]. Урогенитальная инфекция играет ключевую роль в генезе различных патологических процессов при беременности и состоянии здоровья новорожденного . Наиболее частой причиной преждевременных родов является условно-патогенная флора урогенитального тракта. При этом изменение биоценоза влагалища с соответствующим изменением рН может быть использовано как маркер оценки риска преждевременных родов [Радзинский В.Е., Хамошина М.Б., Календжян А.С., 2010]. Преждевременный разрыв плодных оболочек осложняет течение преждевременных родов в 19,95% случаев . Исследования показали, что основной путь изменения оболочек с их последующим разрывом — инфицирование их различными микроорганизмами восходящим путем . Ранняя диагностика преждевременного излития околоплодных вод во многом определяет дальнейшую тактику ведения . Обнаружение протеина-1 , связывающего инсулиноподобный фактор роста во влагалищном отделяемом, служит одним из надежных методов диагностики преждевременного разрыва плодных оболочек . В существующей системе диспансеризации недостаточно проработаны единые методические установки применительно к профилактике преждевременных родов и ограничены возможности применения современных методов их прогнозирования, позволяющих осуществить раннее выявление факторов риска и выбор оптимальной тактики ведения беременности [Радзинский В.Е., Оразмурадова А.А., 2009].
Риск развития идиопатического респираторного дистресс-синдрома у недоношенных детей при сроке гестации менее 28 нед. составляет 60%, от 32 до 36 нед. — 20%, более 37 нед. — 5% . Стероидная терапия глюкокортикоидами на 40% снижает раннюю неонатальную смертность.
Преждевременные роды подразделяются на спонтанные и индуцированные, связанные с состоянием здоровья беременной и/или плода. Спонтанные преждевременные роды, в свою очередь, могут начинаться с регулярной родовой деятельности при целом плодном пузыре — идиопатические (около 40-50% случаев) или с отхождения околоплодных вод при отсутствии родовой деятельности (около 50%) . По клинической картине преждевременные роды делятся на угрожающие, характеризующиеся нерегулярными сокращениями матки и открытием шейки матки до 3-4 см, и начавшиеся — в этом случае наступает регулярная родовая деятельность и происходит открытие шейки матки на 3-4 см и более. Каждый третий случай преждевременных родов происходит у первобеременных, у которых к факторам риска следует отнести ранее перенесенные аборты или самопроизвольные выкидыши, инфекцию мочевыводящих путей, воспалительные заболевания гениталий .
Диагноз начала преждевременных родов сопряжен с определенными трудностями в связи с отсутствием специфической симптоматики. Прогнозирование начала наступления преждевременных родов — это чрезвычайно важная в практическом отношении проблема, поскольку примерно в 50% случаев сократительная деятельность матки спонтанно прекращается . В качестве предиктора преждевременных родов в настоящее время довольно успешно применяется экспресс-тест на определение фосфорилированной формы протеина-1 , диагностическая чувствительность которого равняется 88,9%, а диагностическая специфичность — 100% .
Фосфорилированный протеин-1 , связывающий инсулиноподобный фактор роста, синтезируется децидуальными клетками. Околоплодные воды, сыворотка плода и беременной, напротив, содержат большое количество нефосфорилированного ПСИФР-1 . При приближении срока родов околоплодные оболочки начинают отделяться от децидуальной оболочки, в результате высвобождается небольшое количество фПСИФР-1 . Отрицательный результат указывает на низкий риск преждевременных родов в течение 7 дней после проведения теста. Прогностическая ценность отрицательного результата — 94%.
На первом этапе исследования нами проведен ретроспективный клинико-статистический анализ 137 историй преждевременных родов. Эти исследования проводились по специально разработанной методике обследования, при которой учитывались паспортные, анамнестические, клинические данные, сведения об образовании, о наличии профессиональных вредностей, паритета, особенности течения предыдущих и настоящей беременности и родов, а также о состоянии и исходе родов для плода и новорожденного. Произведено выделение факторов риска и формирование групп высокого риска по преждевременным родам.
На втором этапе, который составил основную часть исследования, было проведено динамическое проспективное наблюдение за 143 беременными от момента их постановки на учет до выписки из стационара после родоразрешения. Данная группа была сформирована на основании данных анкетирования, в процессе которого выяснялись факторы риска преждевременных родов.
Критерии включения: наличие урогенитальной инфекции, диагностированная истмико-цервикальная недостаточность, плацентарная недостаточность и анамнестические факторы (преждевременные роды в анамнезе, множественные внутриматочные вмешательства, преждевременная отслойка плаценты в анамнезе).
Критерии исключения: тяжелая экстрагенитальная патология, многоплодная беременность.
Все наблюдаемые беременные подвергались углубленному клиническому обследованию.
Исходы родов для плода, течение раннего неонатального периода проанализированы у 280 новорожденных. В ходе работы были использованы общеклинические (клинико-анамнестические, лабораторные), специальные (УЗИ, допплерометрия, КТГ), генетические, патолого-анатомические, иммунологические и статистические методы исследования.
Для выполнения задач исследования, включающих использование высокочувствительных тест-систем, основанных на определении протеина-1 , связывающего инсулиноподобный фактор роста во влагалищном отделяемом, из числа обследованных беременных было отобрано 85 пациенток с угрозой прерывания беременности и 29 пациенток с диагностированными мутациями в генах тромбофилии, с последующим применением низкомолекулярного гепарина, ознакомленных с целью и методами исследования, давших письменное согласие на их включение в научное исследование.
Пациентки обеих групп, включенные в исследование, были сопоставимы по возрасту и соматическому здоровью. В ретроспективной группе (РГ) у всех анализируемых пациенток отмечалось осложненное течение беременности (табл. 1).
Анализ факторов риска преждевременных родов в проспективной группе (ПГ) показал сходное распределение частоты рисков, что и в РГ. В обеих группах в трети случаев имело место сочетание факторов риска (R=0,22; р=0,01). Анализируя состояние соматического статуса, стоит отметить, что при хронических заболеваниях почек, а также при состояниях бессимптомной бактериурии роды до 28 нед. происходили в 3 раза чаще (58%), чем на сроке 33-37 нед. — 17% (p<0,01). Влагалищная инфекция в нашем исследовании занимает ключевую позицию, т. к. в 18 случаях роды наступили до 28 нед., что почти в 6 раз превышает таковые показатели при родах на сроке 33-37 нед. (p<0,01). Половина родов на сроке 28-33 нед. происходили на фоне влагалищной инфекции — 51% (p<0,01). При родах в 28-37 нед. предлежание плаценты отмечено в 17,86% случаев.
Аномалии предлежания плаценты наблюдались в 5 раз чаще при преждевременных родах до 28 нед., чем при родах на сроке 33-37 нед. (p<0,01). Преждевременная отслойка плаценты произошла в 23 (16,8%) случаях, на сроке до 28 нед. — 31,6%, на сроке 28-32 нед. 6 дн. — 13,1% и при сроке 33-37 нед. — 17,7% (p<0,01) (рис. 1).
Нами отмечено, что все женщины РГ имели отягощенный акушерско-гинекологический анамнез. Так, у 56,93% женщин были преждевременные роды в анамнезе, у 33,58% отмечено искусственное прерывание беременности или диагностическое выскабливание, а оперативные вмешательства на шейке матки в анамнезе — у 24,82% (табл. 2).
У 54% пациенток РГ беременность протекала с угрозой прерывания на различных сроках, из них стационарную помощь получили 89%. Токолитическая терапия в стационаре проводилась преимущественно препаратами сульфата магния — 54%, β-адреномиметиками — 27%, нестероидными противовоспалительными препаратами — 11%, их сочетание имело место в 7,5% случаев. Терапия β-адреномиметиками и нестероидными противовоспалительными препаратами в сроки до 28 нед. не назначалась.
У ближайших родственников анализируемых беременных в исследовании наследственности были отмечены в 24 случаях инсульты, тромбозы глубоких вен и инфаркты. При изучении анамнеза женщин ретроспективной группы отмечена преждевременная отслойка плаценты в 17% случаев, плацентарная недостаточность с внутриутробной задержкой развития плода — в 53% случаев. У таких пациенток в 63,33% случаев произошли очень ранние преждевременные роды, что в 3 раза чаще, чем роды на сроке 33-37 нед. (R=0,21; р=0,01).
В 63% случаев преждевременные роды до 28 нед. начинались с преждевременного излития околоплодных вод, на сроке 28-32 нед. 6 дн. — в 74%, при родах в 33-37 нед. — в 30% случаев (p<0,02).
Частота преждевременных родов в период 2010—2012 гг. , по данным статистических отчетов, колебалась от 7,8 до 10,6% (рис. 2).
Все беременные ПГ были поставлены на учет до 6-недельного срока гестации, после УЗИ, конкретизирующего срок беременности и место имплантации плодного яйца.
При самостоятельном скрининге на влагалищную инфекцию отклонение в значении рН влагалищного содержимого в ПГ выявлено у 43% беременных. Бактериоскопическое исследование установило, что бактериальный вагиноз имеет место в 37 (59,68%) случаях, вагинальный кандидоз — в 11 (17,74%), неспецифический вагинит — в 14 (22,58%) случаях (p<0,05) (табл. 3).
В ПГ обследование на мутации в системе гемостаза проводилось всем беременным с преждевременными родами в анамнезе — в 59% случаев, преждевременной отслойкой плаценты — в 19%, предлежанием плаценты — в 17% случаев. У трети беременных из 102 обследованных были выявлены мутации в генах системы гемостаза (табл. 4). Все беременные с подтвержденными генетическими мутациями тромбофилии были госпитализированы для дообследования и подбора терапии низкомолекулярными гепаринами.
Пациентки с мутацией в гене MTFHR (С667ТТ) дополнительно во время беременности получали препараты фолиевой кислоты. Оценивался уровень гомоцистеина. Динамический контроль за лечением проводился по показателям гемостазиограммы 1 раз в 2 нед.
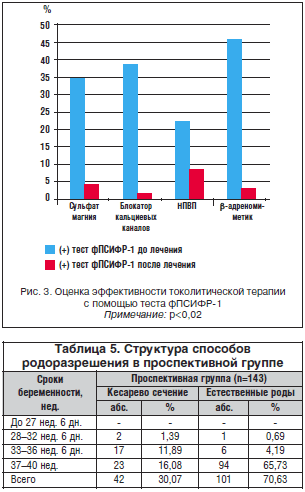
При обращении с жалобами на дискомфорт или боли внизу живота, начиная с 22 нед. гестации, у 85 беременных для диагностики и прогнозирования наступления преждевременных родов использовался высокочувствительный тест на полосках, определяющий фосфорилированную форму протеина-1 , связывающего инсулиноподобный фактор роста. В 53% случаев угрозы прерывания беременности при первом обращении получен положительный результат, подтвержденный УЗИ и мануальным исследованием, данные беременные госпитализированы, 47% пациенток продолжили амбулаторное наблюдение. Оценку качества терапии, угрозы прерывания беременности в стационаре проводили с помощью повторного теста на определение фПСИФР-1 (рис. 3).
Нами отмечено, что при применении β-адреномиметиков частота повторных положительных результатов при тестировании в 2 раза ниже, чем при применении блокаторов кальциевых каналов и НПВП (Р<0,02). По результатам нашего исследования, наиболее предпочтительным для снятия угрозы прерывания беременности на сроке до 28 нед. является блокатор кальциевых каналов — нифедипин, а на сроке 28-33 нед. — сульфат магния и гексапреналина сульфат (р<0,02).
В РГ очень ранние преждевременные роды до 28 нед. гестации имели место в 13,9% случаев, ранние в 28-32 нед. 6 дн. — 61,3% и роды на сроке 33-37 нед. — в 25,8% случаев. В ПГ, благодаря проведенной комплексной профилактике, преждевременные роды на сроке до 28 нед. не произошли. Роды на сроке 28-32 нед. 6 дн. беременности произошли в 2 случаях.
Анализ данных по группам показал, что преждевременные роды на сроке 33-37 нед. в РГ (4,4%) заканчивались кесаревым сечением в 2 раза реже, чем в ПГ (11,9%) (R=0,17; р=0,01) (табл. 5).
У пациенток с наследственной тромбофилией роды через естественные родовые пути на сроке 33-37 нед. произошли в 6,9% случаев (p<0,01), на сроке 37-40 нед. гестации путем кесарева сечения — в 10,3%, через естественные родовые пути — в 79,3% случаев (p<0,01).
В ПГ родились 143 ребенка. Из них на сроке 28-32 нед. 6 дн. — 2,1%, 33-37 нед. — 16,1% и в доношенном сроке — 81,8% детей. Оперативным способом родились 42 ребенка, естественным путем — 101 (рис. 4). В ретроспективной группе на сроке 28-32 нед. 6 дн. ведущими заболеваниями были пневмония — 66,1%, конъюгационная желтуха — 37,3%, респираторный дистресс-синдром мембран — 59,3% (p<0,02). Сравнивая результаты в группах, стоит отметить, что заболеваемость пневмонией и респираторным дистресс-синдромом у недоношенных детей в ПГ снизилась в 4 раза по сравнению с РГ (R=0,17; р=0,02).
В ПГ на первом месте в структуре заболеваемости находился отечный синдром — 21,7%, конъюгационная желтуха — 17,4%, гемолитическая болезнь — 17,4%, пневмония и респираторный дистресс-синдром — по 13,1% (рис. 5).
Сравнивая результаты в группах, стоит отметить, что заболеваемость пневмонией и респираторным дистресс-синдромом у недоношенных детей в ПГ снизилась в 4 раза по сравнению с РГ (R=0,17; р=0,02). В 3 раза снизилось число детей в ПГ (21,7%) нуждающихся в искусственной вентиляции легких, по сравнению с РГ (R=0,21; р=0,02).
Формирование групп высокого риска по преждевременным родам позволяет оптимизировать диагностическую и лечебную тактику. Выявление урогенитальной инфекции с помощью простого теста самодиагностики определения рН влагалищной среды с последующим бактериоскопическим исследованием и санацией позволяет снизить частоту преждевременных родов. Необходимым является определение тромбофилии, и в частности наследственных мутаций генов тромбофилии, с профилактическим применением низкомолекулярных гепаринов. Правильный подбор токолитической терапии с использованием современной высокочувствительной тест-системы, определяющей фосфорилированную форму протена-1 , связывающего инсулиноподобный фактор роста во влагалищном отделяемом, для оценки ее эффективности, способствует снижению частоты преждевременных родов.





Литература
- Акушерство. Справочник Калифорнийского университета / Под ред. К. Нисвандера, А.Э. Эванса / Пер. с англ. М.: Практика, 1999. 703 с.
- Власова Т.А., Вальдман С.Ф., Иванова Н.В. и др. Факторы риска и особенности ведения преждевременных родов // Репродуктивное здоровье женщины. 2000. № 2. С. 153-160.
- Кулаков В.И., Серов В.Н., Сидельникова В.М. Преждевременные роды - тактика ведения с учетом срока гестации // Журнал акушерства и женских болезней. 2002. № 2. С. 13-17.
- Макацария А.Д., Бицадзе В.О., Гениевская М.Г. и др. // Антифосфолипидный синдром в акушерской практике. М.: Руссо, 2003. С. 344.
- Михайлов М.К. Биомеханизм родовых повреждений позвоночника, спинного мозга и позвоночных артерий: методические материалы. Казань, 1994. С. 6-8.
- Сидельникова В.М. Акушерская тактика ведения преждевременных родов // Акушерство и гинекология. 2000. № 5. С. 8-12.
- Сидельникова В.М., Тетруашвили Н.К. Преждевременные роды и иммунологические аспекты // Акушерство и гинекология. 2002. № 7. С. 44-49.
- Федорова М.В. Плацентарная недостаточноть // Акушерство и гинекология. 1997. № 6. С. 40-43.
- 9. Шалина Р.И., Курцер М.А., Плеханова Е.Р. и др. Несвоевременное излитие околоплодных вод: активная и выжидательная тактика ведения преждевременных родов // Вопросы гинекологии, ушерства перинатологии. 2006. Т. 5, № 1. С. 27-32.
- Шалина Р.И., Плеханова Е.Р. Комплексная терапия беременных с угрозой преждевременных родов // Вопросы гинекологии, акушерства и перинатологии. 2007. Т. 6, № 1. С. 33-40.
- 11. Шаповаленко С.А. Комплексная диагностика и лечение плацентарной недостаточности у беременных на разных стадиях гестации // Вестник Росс. ассоциации акушеров-гинекологов. 2001. № 2. С. ‐47.
- Gyetvai K., Hannah M., Hodnett E. et al. Tocolytics for preterm labor: a systematic review // Obstet. Gynecol. 1999. Vol. 94. P. 869-877.
- 13. How H.Y., Cook C.R., Cook V.D. et al. Preterm premature rupture of membranes: aggressive tocolysis versus expectant management // J. Matern. Fetal. Med. 1998. Vol. 7. P. 8-12.
- Mattison D., Damus K., Fiore E. et al. Preterm delivery: a public health perspective // Paediatr. Perinatal. Epidemiol. 2001. Vol. 15. C. 7-16.
- Monaghan S., Little R., Hulchiy O. et al. Preterm birth in two urban areas of Ukraine // Obstet. Gynecol. 2000. Vol. 95. P. 752-755.
- 16. Naef R.W. 3rd , Allbert J.R., Ross E.L., et al. Premature rupture of membranes at 34 to 37 weeks’gestation: aggressive versus conservative management // Am. J. Obstet. Gynecol. 8. Vol. 178. P. 126-130.
- Paternoster D.M., Bertoldini M., Pignataro R. et al. Analisi comparativa dei inarcatori di parto pretermine // Acta biomed. Ateneo parm. 2000. Vol. 71. P.331-356.
- 18. Ramsey P.S., Lieman J.M., Brumfield C.G. et al. Chorioamnionitis increases neonatal morbidity in pregnancies complicated by preterm premature rupture of membranes // Am. J. Obstet. ecol. 2005. Vol. 192 (4). P. 1162-1166.
- Rabe H., Reynolds G.J., Diaz-Rosello J.L. Early versus delayed umbilical cord clamping in preterm infants // Cochrane Library. 2009. Vol. 1.
- Scholl T.O. Iron status during pregnancy: setting the stage for mother and infant // Am. J. Clin. Nutr. 2005. Vol. 81. P. 1218S-1222S.
- Wolf H., Schaap A.H.P., Bruinse H.W. et al. Vaginal delivery compared with caesarean section in early preterm breech delivery: a comparison of long term outcome // Br. J. Obstet. aecol. 1999. Vol. 106. P. 486-491.
Для цитирования:
Серов В.Н., Тютюнник В.Л. Тактика лечения угрожающих преждевременных родов // РМЖ. Мать и дитя. 2008. №19. С. 1252
Преждевременные роды - патологическое состояние, в результате которого рождается не просто недоношенный, но и, как правило, больной ребенок, что является основной причиной перинатальной заболеваемости и смертности.
Преждевременные роды являются одним из самых важных аспектов проблемы охраны здоровья матери и ребенка. На долю недоношенных детей приходится 65-70% ранней неонатальной и детской смертности. Мертворождаемость при преждевременных родах наблюдается во много раз чаще, чем при своевременных. Перинатальная смертность у недоношенных новорожденных в 30-35 раз выше, чем у доношенных.
В России принято считать преждевременными роды, наступившие при сроке от 28 до 37 недель беременности с массой плода 900 г и более. Однако в ближайшие годы в России статистика преждевременных родов, а также перинатальной заболеваемости и смертности будет осуществляться по рекомендациям ВОЗ, согласно которым учет перинатальной смертности осуществляется с 22-й недели беременности с массой плода более 500 г. По этим критериям в США частота преждевременных родов в 2005 году составила 9,7%, в Великобритании - 7,7%, во Франции - 7,5%, в Германии - 7,4%. В связи со сроками беременности, принятыми в нашей стране, частота преждевременных родов колеблется в пределах 5,4-7,7%.
Причины, вызывающие преждевременные роды, являются мультифакторными. Факторами риска преждевременных родов являются как социально-де-мо-графические (неустроенность семейной жизни, низкий социальный уровень, молодой возраст), так и клинические причины. Каждая третья женщина, имеющая преждевременные роды - первобеременная, у которой к факторам риска следует отнести ранее перенесенные аборты или самопроизвольные выкидыши, инфекцию мочевыводящих путей, воспалительные заболевания гениталий. Важную роль в возникновении преждевременных родов играет и осложненное течение данной беременности, механизм развития которого позволяет выделить главные причины.
На основании многолетнего опыта научно-ис-сле-довательской и клинической работы по проблемам привычной потери беременности и преждевременных родов, В.М. Сидельникова выделяет следующие основные причины последних.
. Инфекция - острая и/или хроническая, бактериальная и/или вирусная - являющаяся одной из основных причин.
. Стресс матери и/или плода, обусловленный наличием экстрагенитальной патологии, осложнений беременности и плацентарной недостаточности, что ведет к повышению уровня кортикотропин-рилизинг-гормона плодового и/или плацентарного и, как следствие этого, к развитию преждевременных родов.
. Тромбофилические нарушения, которые ведут к отслойке плаценты, тромбозам в плаценте. Высокий уровень тромбина может провоцировать увеличение продукции простагландинов, активацию протеаз и отслойку плаценты, являющуюся наиболее частой причиной досрочного родоразрешения.
. Перерастяжение матки при многоплодии, многоводии, при пороках развития матки, инфантилизме ведет к активации рецепторов окситоцина и т.д. - и к развитию преждевременных родов.
Нередко имеется сочетание этих факторов в развитии преждевременных родов. Появление симптомов активации сократительной деятельности матки, то есть симптомов угрожающих преждевременных родов, является конечным звеном в сложной цепи активации сократительной деятельности матки. Без знания причин развития преждевременных родов не может быть их успешного лечения. В настоящее время все лечение угрозы прерывания сводится к симптоматическому лечению - использованию средств для снижения сократительной деятельности матки. Это объясняет, почему при огромном количестве различных токолитических средств в нашем арсенале частота преждевременных родов в мире не уменьшается, а снижение перинатальной смертности происходит в основном благодаря успехам неонатологов в выхаживании недоношенных детей.
В связи с вышеизложенным, тактика ведения и лечение угрозы преждевременных родов должны учитывать возможные причины их развития, а не состоять только в назначении симптоматических средств, направленных на снижение сократительной деятельности матки.
Тактика лечения определяется множеством факторов, таких как срок гестации, состояние матери и плода, целостность плодного пузыря, характер сократительной деятельности матки, степень изменений шейки матки, наличие кровотечения и его тяжесть.
Срок беременности тесно связан с причинами преждевременных родов. По рекомендации ВОЗ преждевременные роды делят по срокам гестации на очень ранние преждевременные роды - 22-27 недель гестации, ранние преждевременные роды - 28-33 недели и преждевременные роды - срок гестации 34-37 недель. Это деление обусловлено разной тактикой ведения и различными исходами беременности для плода.
От состояния здоровья матери зависит, возможно ли пролонгирование беременности или ее целесообразно родоразрешить досрочно. Состояние плода оценивается специальными методами: ультразвуковым сканированием, допплерометрическим исследованием кровотока в системе «мать-плацента-плод», кардиотокографией. Если состояние плода позволяет, необходимо пролонгировать беременность хотя бы на время, необходимое для проведения профилактики респираторного дистресс-синдрома плода.
Целостность плодного пузыря имеет большое значение при выборе тактики ведения. При целом плодном пузыре возможна выжидательная тактика и проведение терапии, направленной на пролонгирование беременности. При преждевременном излитии околоплодных вод или высоком боковом разрыве плодного пузыря тактика определяется наличием или отсутствием инфекции, характером предлежания плода и др.
В зависимости от характера и активности сократительной деятельности матки и от степени изменений шейки матки может быть выбрана выжидательная тактика ведения, направленная на пролонгирование беременности. Консервативная тактика возможна при состоянии здоровья матери и плода, позволяющем пролонгирование беременности, при целом плодном пузыре, при раскрытии шейки матки не более 2 см, при отсутствии признаков инфекции.
При выборе выжидательной тактики ведения при угрозе преждевременных родов необходимо:
. решить в каждом конкретном случае, какой вид токолитической терапии следует использовать;
. ускорить «созревание» легких плода путем проведения профилактики респираторного дистресс-син-дрома плода, а также улучшить его состояние;
. определить предполагаемую причину угрозы преждевременных родов (инфекция, плацентарная недостаточность, тромбофилические нарушения, ос-ложнения беременности, экстрагенитальная патология и т.д.) и проводить лечение патологических состояний параллельно с лечением угрозы прерывания.
Различают угрожающие, начинающиеся и начавшиеся преждевременные роды. Для угрожающих преждевременных родов характерны непостоянные боли в пояснице и внизу живота на фоне повышенного тонуса матки. При этом шейка матки остается закрытой. При начинающихся преждевременных родах обычно возникают схваткообразные боли внизу живота, сопровождающиеся регулярным повышением тонуса матки (схватки). Шейка матки при этом укорачивается и раскрывается. При этом нередко происходит и преждевременное излитие околоплодных вод.
Для преждевременных родов характерно: несвоевременное излитие околоплодных вод; слабость родовой деятельности, дискоординация или чрезмерно сильная родовая деятельность; быстрые или стремительные роды или, наоборот, увеличение продолжительности родов; кровотечение из-за отслойки плаценты; кровотечение в последовом и раннем послеродовом периодах вследствие задержки частей плаценты; воспалительные осложнения как во время родов, так и в послеродовом периоде; гипоксия плода.
При возникновении симптомов, указывающих на возможность преждевременных родов лечение должно быть дифференцированным, так как при начинающихся родах может быть проведено лечение, направленное на сохранение беременности. Назначают постельный ре-жим, успокаивающие средства, спазмолитические препараты и т.д. К основным лекарственным препаратам, позволяющим успешно противостоять несвоевременному прерыванию беременности, принадлежат токолитические препараты, или токолитики. К ним относятся все медикаментозные средства, которые расслабляют мускулатуру матки. Этих препаратов сейчас много, и на основании исследований сократительной деятельности миометрия предлагаются все новые средства, часть из которых находится в стадии клинических испытаний. Следует отметить, что поиск новых средств обусловлен тем, что не снижается частота преждевременных родов, эффективность многих токолитиков невысока и имеется много побочных действий на мать и плод.
Тем не менее использование токолитических средств чрезвычайно важно и актуально, так как они, хотя и не уменьшают частоту преждевременных родов, но тормозят сократительную деятельность матки, способствуют пролонгированию беременности, позволяют провести профилактику респираторного дистресс-син-дрома плода и т.д.
К одним из наиболее эффективных токолитических препаратов относятся?-миметики - лекарственные средства, используемые для лечения угрозы прерывания после 24-25 недель беременности или преждевременных родов более 30 недель. Препараты этого ряда (ритодрин, Гинипрал, сальбутамол и др.) являются производными эпинефрина и норэпинефрина, освобождающихся при стимуляции симпатических нервных окончаний, и их иногда в литературе называют симпатомиметиками или адренергетиками. Действие?-ми-метиков осуществляется через?-рецепторы. Стиму-ляция?-рецепторов ведет к сокращениям гладкой мускулатуры, а?-рецепторов - к противоположному эффекту: к расслаблению мускулатуры матки, сосудов, кишечника. Наличие?-рецепторов в других тканях (в частности, в мускулатуре сердца) определяет частоту тяжести побочных действий?-миметиков. ?-рецепторы делят на?1- и?2-рецепторы. Токолитический эффект обеспечивается путем воздействия через?2-рецепторы на матку, бронхи, кишечник, а также на образование гликогена в печени и инсулина в поджелудочной железе. На?-рецепторы сердечно-сосудистой системы их влияние менее выражено.
Механизм действия?-миметиков проявляется через адренергическую стимуляцию, что ведет к увеличению образования циклического аденозинмонофосфата (цАМФ) из АТФ путем активации фермента аденилатциклазы. За счет действия цАМФ осуществляется обратный выход Са2+ из клеток в депо и расслабление гладкой мускулатуры. ?-миметики вызывают увеличение потока крови через ткани и органы, повышение перфузионного давления и снижение сопротивления сосудов. Действие на сердечно-сосудистую систему проявляется возрастанием частоты сердечных сокращений, уменьшением систолического и диастолического давления. Такой кардиотропный эффект?-миметиков необходимо учитывать при проведении терапии этими препаратами, особенно при их взаимодействии с другими лекарственными средствами. Перед введением?-миметиков необходимо контролировать уровень артериального давления и частоту пульса. Для снижения побочных сердечно-сосудистых действий обязательно назначают блокаторы кальциевых каналов - финоптин, изоптин, верапамил. Как правило, соблюдение правил использования?-миметиков, режима дозирования, четкий контроль за состоянием сердечно-сосудистой системы позволяют избежать серьезных побочных эффектов.
К дополнительным эффектам от применения?-миметиков относятся: увеличение объема циркулирующей крови и частоты сердечных сокращений, а также снижение периферического сосудистого сопротивления, вязкости крови и коллоидно-онкотического давления плазмы.
В последние годы получены данные о том, что при длительном использовании?-миметиков наблюдается снижение их эффективности. Кроме того, ?-адрено-рецепторы чувствительны со сроков беременности 24-25 недель; в более ранние сроки беременности эффект от их применения не столь выражен. Если угроза преждевременных родов сопровождается повышением тонуса матки, а не схватками, то эффект от применения?-миметиков невысок, так как они снижают контрактильную активность матки, а тонус снижается очень медленно.
В России наиболее распространенным и часто используемым препаратом из группы?-миметиков является Гинипрал - гексопреналин. Это селективный?2-симпатомиметик, расслабляющий мускулатуру матки. Под его воздействием уменьшается частота и интенсивность сокращений матки. Препарат угнетает самопроизвольные, а также вызванные окситоцином родовые схватки; во время родов нормализует чрезмерно сильные или нерегулярные схватки. Под действием Гинипрала в большинстве случаев преждевременные схватки прекращаются, что, как правило, позволяет пролонгировать беременность до доношенного срока. Вследствие своей?2-селективности Гинипрал оказывает незначительное действие на сердечную деятельность и кровоток беременной и плода.
Гинипрал состоит из двух катехоламиновых групп, которые в организме человека подвергаются метилированию посредством катехоламин-О-метил-трансфе-разы. В то время как действие изопреналина почти полностью прекращается при введении одной метиловой группы, гексопреналин становится биологически неактивным только в случае метилирования обеих своих катехоламиновых групп. Это свойство, а также высокая способность препарата к адгезии на поверхности считаются причинами его продолжительного действия.
Показаниями к применению Гинипрала являются:
. Острый токолиз - торможение родовых схваток во время родов при острой внутриматочной асфиксии, иммобилизация матки перед кесаревым сечением, перед поворотом плода из поперечного положения, при пролапсе пуповины, при осложненной родовой деятельности. Как экстренная мера при преждевременных родах перед доставкой беременной в больницу.
. Массивный токолиз - торможение преждевременных родовых схваток при наличии сглаженной шейки матки и/или раскрытия зева матки.
. Длительный токолиз - профилактика преждевременных родов при усиленных или учащенных схватках без сглаживания шейки или раскрытия зева матки. Иммобилизация матки до, во время и после хирургической коррекции истмико-цервикальной недостаточности.
Противопоказания к назначению данного препарата: гиперчувствительность к одному из компонентов препарата (в особенности больным, страдающим бронхиальной астмой и гиперчувствительностью к сульфитам); тиреотоксикоз; сердечно-сосудистые заболевания, особенно нарушения ритма сердца, протекающие с тахикардией, миокардит, порок митрального клапана и аортальный стеноз; ишемическая болезнь сердца; тяжелые заболевания печени и почек; артериальная гипертензия; внутриматочные инфекции; лактация.
Дозировка. При остром токолизе применяют 10 мкг Гинипрала, разведенных в 10 мл раствора натрия хлорида или глюкозы (вводить в течение 5-10 мин. медленно внутривенно). При необходимости продолжить введение путем в/в инфузий со скоростью 0,3 мкг/мин. (как при массивном токолизе).
При массивном токолизе - в начале 10 мкг Гини-прала медленно внутривенно, затем - внутривенная инфузия препарата со скоростью 0,3 мкг/мин. Можно вводить препарат со скоростью 0,3 мкг/мин. и без предварительной в/в инъекции. Вводить в/в капельно (20 капель=1 мл).
Как первую линию помощи при угрозе прерывания после 24-25 недель беременности или угрозе преждевременных родов Гинипрал назначают из расчета 0,5 мг (50 мкг) в 250-400 мл физиологического раствора внутривенно капельно, постепенно увеличивая дозу и скорость введения (максимально 40 капель/мин.), совмещая инфузию с приемом блокаторов кальциевых каналов (финоптин, изоптин, верапамил) под контролем частоты пульса и параметров артериального давления. За 20 минут до конца внутривенного вливания 1 таблетка Гинипрала (5 мг) per os через каждые 4 часа.
Снижение дозы Гинипрала необходимо проводить после полной ликвидации угрозы прерывания, но не менее чем через 5-7 дней (уменьшить дозу, а не удлинить промежуток времени между приемом дозы препарата). На основании многолетнего использования Гинипрала установлено, что эффективность его применения составляет около 90%.
Таким образом, накопленный десятилетиями отечественный и зарубежный опыт свидетельствуют о том, что несмотря на все возрастающий арсенал токолитических средств, на сегодняшний день нет более эффективных средств для подавления сократительной деятельности матки, т.е. угрозы преждевременных родов, чем?-миметики, и, в частности, Гинипрал.

